多发性硬化症(MS)是一种中枢神经系统慢性炎症性疾病,可导致脑炎和脱髓鞘发生。MS被认为是一种自身免疫性疾病,由自身反应性T细胞引起,症状包括肌肉僵硬和麻痹、视觉障碍和失明、感觉丧失和共济失调,具有反复复发的特征。目前有多种不同的MS动物模型,其中实验性自身免疫脑脊髓炎(EAE)模型由于具有和MS相似的炎症和脱髓鞘的病理特征,被广泛应用于多发性硬化症的研究。
在小鼠、大鼠等啮齿类动物中,可使用脊髓匀浆、纯化的髓鞘、髓鞘蛋白(如髓磷脂碱性蛋白MBP、蛋白脂蛋白PLP和髓鞘少突胶质细胞糖蛋白MOG)或这些蛋白的肽免疫诱导产生EAE模型。这可能是由于髓磷脂特异性T细胞在外周被激活,穿过血脑屏障进入中枢神经系统并被重新激活,引发一系列炎症反应,导致脱髓鞘和轴突细胞凋亡,最终导致神经损伤和失去功能。使用标准化评分系统评估临床症状,可衡量疾病的诱导发生程度,在病理组织染色切片中可见局部脱髓鞘和炎性白细胞浸润。
云顶国际在野生C57BL/6小鼠和自主开发的B-hIL17A人源化小鼠上建立了MOG诱导的EAE疾病模型,可用于MS相关药物的药效评价。
在C57BL/6小鼠中诱导EAE疾病模型及小分子药效研究
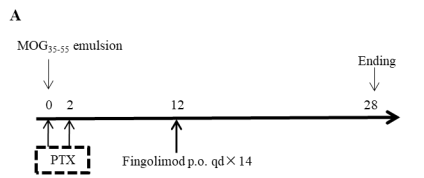
模型构建示意图

临床评分

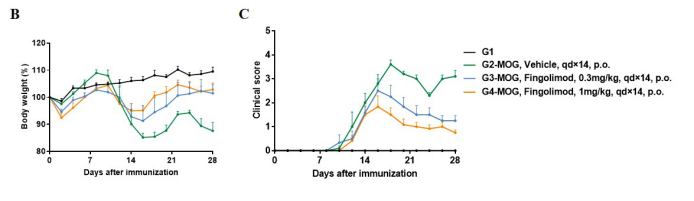
在10周龄C57BL/6雌性小鼠(n=6)中使用MOG35-55乳剂免疫,在免疫当天和第二天分别给与PTX,在免疫后12天口服给药不同剂量的小分子药芬戈莫德(图A),记录各组动物体重变化百分比(图B),并对各组动物临床表现进行评分(图C)。结果显示,与对照组(G1)相比,MOG35-55免疫的小鼠(G2-G4)表现出尾巴无力、跛行、后肢瘫痪和其他症状,临床评分显著增加,这说明在野生型C57BL/6小鼠成功诱导了EAE疾病模型。服用小分子药芬戈莫德后,观察到临床症状以剂量依赖性方式减缓。数据显示为平均值±SEM。MOG35-55:髓鞘少突胶质细胞糖蛋白多肽35和55。PTX:百日咳毒素。Fingolimod:芬戈莫德。
病理分析
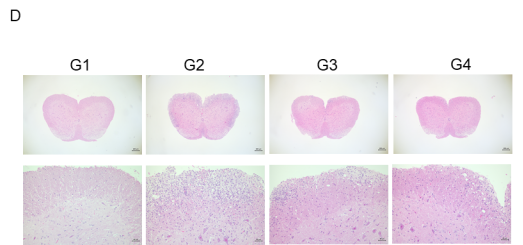


EAE模型小鼠的中枢神经系统(CNS)的局部炎症反应。在MOG35-55和PTX免疫后第28天取脊髓,对组织切片进行苏木精和伊红染色(图D),并对脊髓中浸润的炎性细胞进行评分(图E)。与对照组(G1)相比,MOG35-55免疫小鼠(G2-G4)的炎症细胞浸润显著增加,这进一步证明在野生型C57BL/6小鼠中成功诱导EAE。服用芬戈莫德后,炎症细胞浸润明显受到抑制。数值以平均值±SEM表示。
|
产品名称 |
产品编号 |
|
B-hIL17A mice |
110053 |
|
B-hTNFA mice |
110002 |
参考文献:
1. Gaffen, S.L., Jain, R., Garg, A.V. & Cua, D.J. The IL-23-IL-17 immune axis: from mechanisms to therapeutic testing. Nat Rev Immunol 14, 585-600 (2014).
2. Iwakura, Y. & Ishigame, H. The IL-23/IL-17 axis in inflammation. J Clin Invest 116, 1218-1222 (2006).
3. Kuwabara, T., Ishikawa, F., Kondo, M. & Kakiuchi, T. The Role of IL-17 and Related Cytokines in Inflammatory Autoimmune Diseases. Mediators Inflamm 2017, 3908061 (2017).



 京公网安备: 11011502005564号
京公网安备: 11011502005564号






